|
 El
precedente: CRD electrónico El
precedente: CRD electrónico
El cuaderno
de recogida de datos electrónico se ha venido implantando
en los últimos años como una alternativa cada vez
más eficaz a la tradicional recogida de datos en papel. De
este modo se evitan las pérdidas de tiempo derivadas de la
necesidad del transporte físico de la documentación
en papel hasta un centro de proceso de datos, la inserción
de éstos en documentos electrónicos y su posterior
depuración. Mediante el CRD electrónico la base de
datos es alimentada directamente por el investigador o sus colaboradores
y el proceso de depuración se halla implementado en la propia
herramienta de recogida electrónica de datos.
No es la primera
vez que Bristol-Myers, compañía líder a nivel
mundial en el sector farmaceútico y con más de cincuenta
líneas de productos, utiliza la transmisión electrónica
de datos para la recogida de información de sus estudios.
Con anterioridad a esta experiencia piloto el grupo BMS está
llevando a cabo la recogida de datos de este modo contando con la
colaboración de Phidea como soporte de consultoría
tecnológica integral para Investigación Clínica.
El ensayo clínico en el que se está aplicando esta
tecnología, es en el área cardiovascular, en la que
Bristol-Myers es líder en España y Europa, al igual
que en antivirales y oncología, siendo la sexta compañía
farmacéutica a nivel mundial.
La novedad:
Tecnología móvil GPRS
De cualquier
modo, la recogida remota de datos mediante CRD electrónico
no deja de presentar la desventaja para el investigador de la recogida
de datos en papel sobre cada paciente y su posterior transcripción
sobre la base de datos, con la pérdida de tiempo que ello
conlleva. Igualmente la necesidad de contar con un ordenador conectado
a la red telefónica limita de gran manera la capacidad operativa
del investigador.
En el experimento
piloto que se lleva a cabo se utilizan terminales móviles
con tecnología GPRS conectados a ordenadores de bolsillo
de este modo el investigador puede recoger, en la consulta o incluso
a pie de cama, la información relativa a cada paciente, de
modo que ésta es transmitida rápidamente a la base
de datos central.
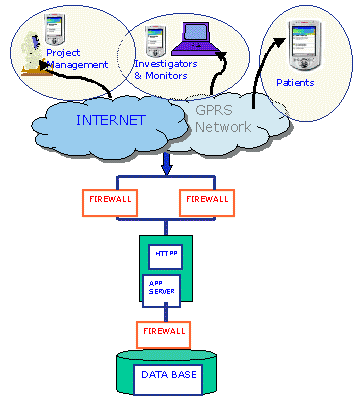
La información
recogida en los centros hospitalarios que participan en estos estudios
se transmite de manera inmediata por medio de la red GPRS de Amena
y a través de Internet a una base de datos centralizada donde,
en tiempo real, el responsable del proyecto podrá disponer
de todos los datos referentes a su estudio.
 La
sinergia entre compañías La
sinergia entre compañías
Para llegar
a este acuerdo ha sido necesaria la colaboración de varias
empresas pertenecientes a diferentes sectores además de una
intensa labor de coordinación entre las diversas culturas
de todas las compañías participantes cuyo resultado
ha sido vital para poner el proyecto en vías de ejecución.
A este nivel,
Phidea ha efectuado un papel de enlace entre los diversos integrantes
del proyecto, canalizando la información de cada uno de éstos
hacia los otros sectores y sirviendo de nexo entre los diferentes
intereses de cada uno.
La tecnología
La interfase
de usuario es extremadamente simple y asegura en todo momento la
calidad de los datos mediante sistemas de filtros que apoyan o complementan
los criterios de selección del estudio. De este modo, podemos
tener la seguridad de que el tiempo empleado a la finalización
de éste en la depuración de los datos será
notablemente menor que en un estudio tradicional.
Adicionalmente
a esto, la necesidad tanto de acceso inmediato de los investigadores
a la base de datos central para insertar o modificar datos, como
la del responsable del proyecto para acceder a tales datos y poder
realizar un seguimiento efectivo del estudio hacen necesario que
la base de datos se halle protegida en todo momento tanto de posibles
pérdidas de información como de acceso por parte de
elementos no autorizados.
Para ello se cuenta con un sistema cuya totalidad de elementos es
redundante de cara a una posible caída, más un complicado
sistema de encriptación en 40 ó 128 bits que hacen
que la transmisión de los datos sea doblemente segura; cumpliendo
todos los requisitos de confidencialidad y seguridad establecidos
por la Ley Orgánica de Tratamiento Automatizado de Datos
(LORTAD) ) y la Ley Orgánica de protección de Datos
(LOPD). Además se ha garantizado el cumplimiento de las más
estrictas normativas internacionales ICH y FDA.
Igualmente,
la aplicación para la captura remota de datos cuenta con
una estructura modular que permite construir aplicaciones a medida
para cada estudio de modo que se pueden aprovechar los desarrollos
de cada módulo para futuras ocasiones lo que reduce drásticamente
los costes a medio plazo.
Los costes
Esta reducción
de costes a medio plazo se hace aún más patente al
referirse a los costes de la transmisión de datos. Una gran
ventaja de la utilización de la red GPRS de Amena es que
permite mantener una conexión contínua sin coste alguno.
La facturación se establece en virtud de la cantidad de información
enviada y recibida, de modo que se cuenta con la comodidad de poder
trabajar sin estar pendiente del reloj.
Las ventajas
El resumen de
las ventajas de esta nueva metodología se puede resumir en
tres aspectos: calidad, tiempo y costes.
En cuanto a
calidad las mejoras más importantes son una mejor inclusión
de pacientes verificable inmediatamente, un mayor control de la
información gracias a los filtros y a la monitorización
en tiempo real, y una reducción de la cantidad de errores
que puede alcanzar un 80% a un 90%.
Los tiempos
que se van a ver acortados son esencialmente los de puesta en marcha,
cierre de la base de datos y análisis estadístico,
además de la optimización del dedicado a la monitorización.
Esto podría suponer un acortamiento de plazos de hasta un
25%
Por último,
aunque no menos importante, la reducción de gastos en algunas
tareas como la impresión, envíos de material y correspondencia
e introducción de datos neutraliza los costes de desarrollo;
y como aspecto estratégico la apuesta por estas tecnologías
se verá beneficiada por una economía de escalas que
puede llegar a suporner un ahorro de entre un 20% y un 40% de los
costes actuales.
Acerca de
Bristol-Myers Squibb
BMS es una compañía estadounidense que comercializa
productos para la salud y cuya misión es mejorar y prolongar
la vida humana. Sus inversiones en I+D ascienden a 2.124 millones
de dólares, prueba del fuerte compromiso que BMS mantiene
con la investigación. Su cartera de productos abarca los
grandes problemas de la salud de nuestro tiempo: hipertensión,
diabetes, cáncer, hipercolesterolemia, ictus, insuficiencia
cardiaca o VIH/SIDA.
Algunos de sus
medicamentos se han convertido en la piedra angular del tratamiento
de enfermedades como el cáncer (TAXOL), la infección
por VIH (VIDEX) o el colesterol elevado (LIPEMOL). En estos momentos,
BMS trabaja en el desarrollo de productos innovadores en otras áreas,
como sistema nervioso central (ABILITAT ) o hipertensión
arterial (VANLEV). La adquisición, el pasado año,
de DuPont Pharma ha venido a reforzar las áreas en las que
ya operaba, como cardiovascular o antirretrovirales. La compañía,
que ocupa la sexta posición en el mundo, cuenta con 44.000
empleados. En España, el Grupo Bristol-Myers Squibb tiene
una plantilla de más de 900 empleados y cuenta con dos fábricas,
una de medicamentos y otra de productos de ostomía, ambas
situadas en Barcelona.
Acerca de Phidea
El grupo Phidea fue fundado en Milán en el año 1982
para la prestación de servicios de I+D+I en la Investigación
Clínica. Desde su implantación en 1991, a la actualidad,
Phidea España cuenta con alrededor de 50 personas entre las
que se encuentran farmacéuticos, biólogos, médicos,
químicos, estadísticos y economistas.
A lo largo de
estos años, Phidea ha adquirido una gran experiencia en Investigación
Clínica y es una de las compañías líderes
dedicada a la Investigación y más decididamente orientada
a la integración a través de las nuevas tecnologías.
Phidea se ha
embarcado en diversos proyectos de implementación de las
nuevas tecnologías en diversas áreas del sector farmaceutico,
y ha estado presente desde el primer momento en el proyecto de GPRS
para ensayos clínicos ejerciendo primero de cabeza de puente
entre los diversos participantes y ocupándose de dar soporte
al estudio piloto tanto en la parte de Investigación Clínica
como la de Biometría, tras la obtención de la base
de datos final.
|